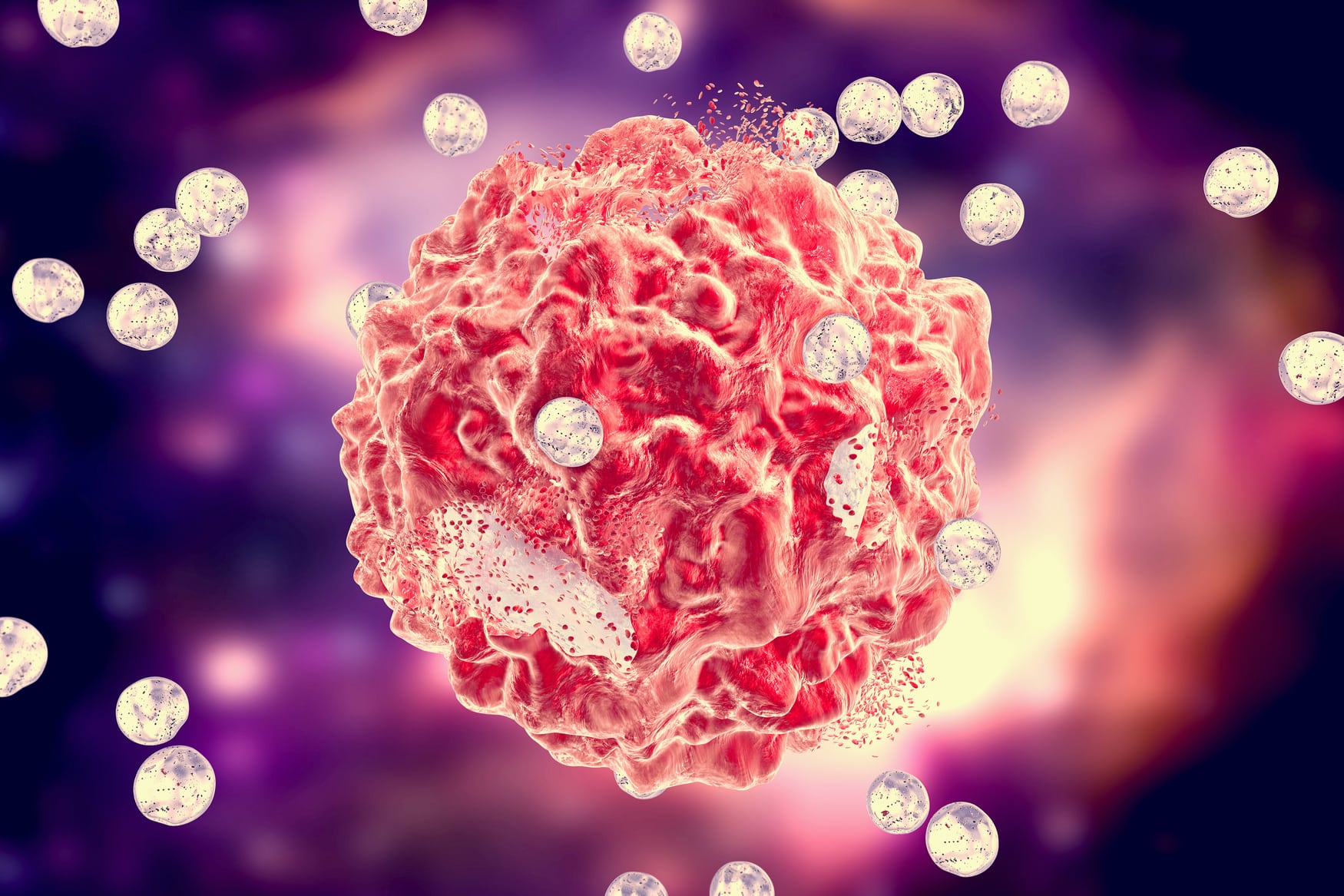
Meskipun terdapat kemajuan pesat dalam proses diagnosis dan terapi keganasan, angka mortalitas tetap menjadi tantangan utama yang dihadapi pada sistem kesehatan. Lingkungan mikro tumor (TME) menyediakan kondisi yang baik untuk sel kanker yang mengakibatkan terjadinya perkembangan hingga metastasis. TME terdiri atas fibroblast, sel imun, matriks ekstraseluler, sel endotel, sitokin, dan faktor-faktor lainnya; yang masing-masing memiliki fungsi khusus dalam proses perkembangan tumor.
Perubahan epigenetik dan mutasi genetik dapat mengakibatkan perkembangan kanker. Kondisi keganasan ini memiliki beberapa karakter khusus, seperti kegagalan dalam merespon sinyal inhibisi pertumbuhan, proliferasi yang tidak terkontrol, proliferasi secara spontan, tidak melalui apoptosis, angiogenesis, dan metastasis, yang masing-masing memiliki peran esensial dalam perkembangan tumor. Selain itu, interaksi komponen stromal pada TME dengan sel tumor memiliki efek yang signifikan dalam perkembangan tumor dan mampu memberikan kondisi yang baik untuk sel kanker berkembang. TME tersusun atas beberapa komponen, seperti sel endotel, perisit, fibroblas, matriks ekstraseluler, dan leukosit. Penelitian menunjukkan bahwa massa kanker berasal dari akumulasi sel keganasan dalam jumlah banyak. Hal ini juga didukung dengan sel tumor yang mampu secara efektif merekrut berbagai sel imun, sel vaskular, dan sel stroma melalui pelepasan sitokin, kemokin, dan faktor pertumbuhan. Sel yang direkrut memiliki potensi untuk melepaskan metabolit intermediat, sinyal yang memicu pertumbuhan, dan komponen perbaikan jaringan untuk membentuk lingkungan mikro. Interaksi antara TME dan sel kanker mampu memicu peningkatan proliferasi, kemampuan metastasis, hingga kematian. Berbagai faktor yang memegang peranan penting dalam perkembangan kanker berkaitan dengan TME, seperti proliferasi dan mekanisme inhibisi apoptosis, angiogenesis yang mencegah terjadinya hipoksia, penekanan sistem imun, dan lingkungan sekitar yang telah dipersiapkan secara optimal sehingga sel tumor dapat menginvasi jarangan sekitarnya dan metastasis.
Pendekatan terbaru dalam melakukan terapi terkait penghantaran obat yang ditemukan bertujuan untuk meningkatkan efisiensi terapi dan memodulasi TME. Pada dekade saat ini, partikel nano digunakan secara luas dalam penghantaran obat, bukan hanya karena bersifat biokompatibel, melainkan juga dikarenakan dapat sekaligus menjaga konsentrasi obat di dalam darah dan melepas substansi obat menuju jaringan yang dituju. Oleh karena itu, pendekatan pengobatan yang ditargetkan dengan partikel nano emas (AuNPs), memiliki sifat yang unik, seperti penyerapan yang dapat diterima, muatan obat dan ligan, imunogenisitas rendah, permeabilitas tinggi, sitotoksisitas tinggi untuk sel tumor, dan partikel penyusun yang mudah dimanipulasi, memiliki hasil yang signifikan dalam pengobatan kanker.
Metode dan Hasil
Pada penulisan ini, kami mendiskusikan lebih ke arah aspek TME dan metode target terapi berkaitan dengan AuNPs. Pendekatan ini dijelaskan berdasarkan karakteristik selular dan fisiologis dari TME, seperti hipoksia, vasa tumor, komponen stroma, dan sel yang terkait. AuNPs merupakan transporter obat yang mendapatkan perhatian lebih dikarenakan karakter hidrofilik, daya angkut yang lebih tinggi, toksisitas lebih rendah, dan bersifat non-imunogenik.
Saat pertumbuhan tumor, bagian dalam dari massa kanker tidak dapat mengakses sistem peredaran darah, sehingga menyebabkan lingkungan hipoksia. Tekanan oksigen dalam darah vena adalah 40 mmHg, sedangkan pada sebagian besar tumor padat, angka ini turun di bawah 5 mmHg dengan bantuan angiogenesis. Hipoksia dapat menyebabkan perubahan fisiologis pada tekanan cairan interstisial, peningkatan produksi ROS, dan penurunan pH. Selain itu, di daerah hipoksia, tekanan cairan interstisial meningkat secara signifikan karena kebocoran arteri dan drainase limfatik abnormal pada tumor. Adanya hipoksia TME, diikuti konsentrasi asam laktat dan asam karbonat meningkat melalui jalur glikolisis, yang menyebabkan penurunan pH. Peningkatan ROS dalam sel menyebabkan kerusakan oksidatif DNA serta mengganggu struktur genom, konsekuensinya adalah tumorigenesis. Namun demikian dalam sel tumor juga menunjukkan peningkatan ekspresi protein antioksidan. Di sisi lain, penghilangan tumor supresor dapat menyebabkan produksi ROS.
Studi pada molekul reaktif NO telah terindentifikasi memiliki dua peran yang berlawanan. Pertama yaitu bahwa tingkat NO yang tinggi dalam TME menyebabkan stres oksidatif, yang mengakibatkan kerusakan DNA, peningkatan apoptosis, dan gangguan fungsi mitokondria. Di sisi lain, tingkat NO yang rendah dapat merangsang angiogenesis dan memiliki sifat anti-apoptosis.
Simpulan
Pertumbuhan kanker membutuhkan substrat yang sesuai dan tersedia pada TME. Selain itu, kondisi lokal TME, termasuk hipoksia, pH asam, ROS, dan oksida nitrat, penting selama proses tersebut. Semua komponen TME seperti ECM, enzim, sitokin, dan sel imun yang terlibat dalam progresi tumor, mengaktifkan jalur sinyal, ekspansi tumor, bahkan metastasis dapat ditargetkan dan dihambat oleh obat atau ligan yang sesuai. Strategi penghantaran obat secara selektif melalui partikel nano, khususnya AuNPs, memiliki keunggulan lebih dibandingkan dengan pengobatan konvensional, seperti kemoterapi dan terapi radiasi. Menurut hasil studi literatur ini, diharapkan adanya kemajuan dalam ilmu kedokteran nano, dimana partikel nano akan menempati sebagai pilihan utama dalam pengobatan kanker.
Penulis: Dr. Hendrik Setia Budi, drg., M.Kes.
Informasi detail dari riset ini dapat dilihat pada tulisan kami di:
https://www.tandfonline.com/doi/abs/10.1080/1061186X.2022.2032095?journalCode=idrt20
Negah Mahhengam, Kimia Kazemnezhad, Hendrik Setia Budi, Mohammad Javed Ansari, Dmitry Olegovich Bokov, Wanich Suksatan, Lakshmi Thangavelu & Homayoon Siahmansouri. Targeted therapy of tumour microenvironment by gold nanoparticles as a new therapeutic approach. J Drug Target . 2022 Feb 2;1-17. doi: 10.1080/1061186X.2022.203209